ヒスチジン:化学式
私の人生の少なくとも一度は、その食べ物。ここで、例えば体に必要なさまざまな物質の日々の量は、どのように食物とともに私たちにもたらされますか?どんなアミノ酸が必要なの?今日では、もちろん、適切な栄養については話しません。なぜなら、このための十分な1つの記事と12の記事がないからです。私たちは生物については間違いなく、非常に重要な物質についてのみ教えていきます。これはアミノ酸ヒスチジンである。その化学名はL-2-アミノ-3-(1H-イミダゾール-4-イル)プロパン酸と複雑に聞こえる。しかし、すべてを順番に。
アミノ酸とは何ですか?
ヒスチジンおよびそのヒスチジンの性質を議論する前に身体の役割、私たちは "アミノ酸"の概念を理解します。スポーツを好む人は、これらの物質について聞いた。アミノ酸は、それを特別にする2つの塩基性官能基を有する有機化合物である:アミノ基-NH2 いわゆるカルボキシル基-COOHである。
最初のものは、この基本的なプロパティを担当しています珍しい種類の化合物。窒素とその電子対のおかげで、アミノ酸は正に荷電したイオンを形成することができる。この場合、アミノ基は、このようなイオン:-NH3+.
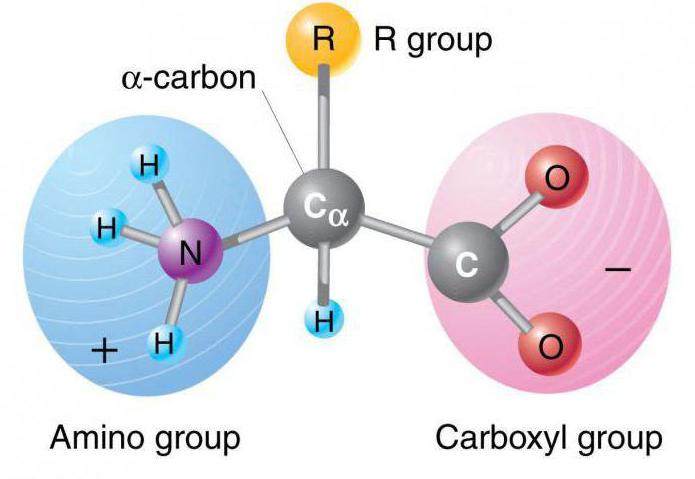
第2の官能基は酸の性質を担う。陽子をあきらめてアニオンになる-COO-。この現象は、カルボキシル基から塩を形成することを可能にする。
したがって、アミノ酸は2つの部分を有し、それぞれが塩を形成することができる。それらの1つは、酸の性質を有するこれらの化合物と、塩基を有する他の化合物とを提供する。一般に、アミノ酸は以下のように表すことができる:NH2-CH(R)-COOHである。 文字Rは、ここでは「ラジカル」、すなわち、官能基および炭素骨格からなり、アミノ酸分子の塩基との結合(または結合)を形成することができる有機粒子であると理解されるべきである。
原則として、慣れていない人薬理学を勉強し、少なくとも一度は広告からでも、アミノ酸が必要であり、非常に有用であると聞いたことがあるスポーツに関与しなかった。彼らが体内でどのような機能を果たしているのか、それを食べ物から必要な割合で得る必要があるのかを考えてみましょう。
体内のアミノ酸の機能
ご存知のように、私たちはすべてタンパク質、脂肪、炭水化物。私たちは生存率を維持するために食べ物を消費します。しかし、この記事の主題では、タンパク質にのみ興味があります。これらは、物質輸送、新しい細胞の創造、脳のニューロン間の結合の強化など、私たちの体内で完全に異なって非常に重要な機能を果たす巨大分子です。

ヒスチジン
任意のアミノ酸の式は、すでにわかっているように少なくとも2つの官能基およびそれらを結合する炭素骨格を発見した。だからこそ、すべてのアミノ酸の違いは、2つのグループ間の炭素架橋の長さとそれに付随するラジカルの構造にあります。

私たちの記事の話題は、アミノ酸の一つです - ヒスチジン。この置き換えられない酸の式は単純ではありません。 2つの官能基間の主な炭素鎖には、1つの炭素原子のみが見られます。実際、必須のタンパク質形成性(タンパク質を生成することができる)アミノ酸はすべて、この鎖中にただ1つの炭素原子を有する。さらに、ヒスチジンは、サイクルを含む複雑なラジカル構造を有する。あなたの上にヒスチジンが何であるかを見ることができます。構造的特徴が複素環(炭素以外の他の原子を含む)である式は、実際には最も複雑な物質ではない。
ですから、基本概念を分析したら、ヒスチジンで行うことができる反応に移ります。
化学的性質
このアミノ酸が入る反応、非常に少ない。酸および塩基との反応に加えて、それはビウレット反応に入り、着色生成物を形成する。さらに、イミダゾール残基を含む式であるヒスチジンは、Pauli反応においてスルファニル酸と相互作用することができる。

結論
おそらく、我々はすべての主要な細部を分解した。この記事はあなたに役立ち、新しい知識を与えてくれることを願っています。



